Токсикологічні досягнення традиційної медицини в 2019 році
Mar 15, 2022
Контакти:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Основні моменти
У статті розглянуто дослідження щодо токсикології традиційної медицини (традиційної медицини) та активних натуральних продуктів протягом останніх 12 місяців, і виявлено, що печінка,ниркаі серце є основними токсичними органами-мішенямитрадиційна медицина. На додачу. у 2019 році почали зосереджувати увагу на безпеці ліків для матері та дитини. Оцінка безпеки Aconitum Carmichael Debx, Tripterygium Wilford Hook.f, Srychnos nux-vomica L, Fallopia multiflora (Thumb.) Harald тощо все ще є гарячою проблемою .

цистанчеможе лікуватинирказахворювання покращує роботу нирок
Традиційність
У цьому щорічному огляді узагальнено нову технологію токсикологічних досліджень, загальні оцінені моделі токсичних органів-мішеней, оцінку безпекиНародна медицинау різних типів людей, а також популярні дослідницькі питання та трави у 2019 році. Порівняно з 2018 роком, багато країн, як-от Австралія, Німеччина та Великобританія, почали звертати увагу на оцінку безпекиНародна медицина.

Токсикологічні досягнення традиційної медицини в 2019 році
Анотація
Було багато типів досліджень, які стосувалися токсикологіїтрадиційна медицината активних натуральних продуктів протягом останніх 12 місяців. У цьому щорічному токсикологічному огляді узагальнено цільові органи традиційної медицини, такі як печінка,нирка, і серце. Безпека препаратуНародна медицинастосується різних типів людей, включаючи немовлят, дітей, період вагітності та післяпологовий період, крім гризунів. Ембріони рибок даніо вважалися загальноприйнятими моделями для оцінки безпеки традиційної медицини. Нові технології в токсикології зосереджені на швидкому скринінгу та ідентифікації токсинів уНародна медицина. Для пояснення механізму гепатотоксичності, спричиненої традиційною медициною, використовується мультиспектральна оптико-акустична томографія, яка відображає точне місце пошкодження печінки, спричиненого традиційною медициною, з 3D-інформацією та інтеграцією екзосомальних мікроРНК сироватки та профілів мікроРНК печінки. Загалом слід звернути увагу на дослідження механізму токсичності інших органів-мішеней, безпеки ліків у людей похилого віку, нових моделей і методів у профілактиці токсикології традиційної медицини в майбутньому.
Ключові слова:Народна медицина, Натуральний продукт, Трава, Токсичність, Токсичні органи-мішені, Оцінка ризику, Оцінка безпеки

Фон
Безпека, ефективність і контроль якості належать до трьох основних характеристик лікарських засобів. У 2019 році з’явилася низка робіт, які стосувалися оцінки безпеки токсинів [1], таких як метал [2], розподіл елементів [3], токсичних білків [4, 5] та спеціальних вторинних метаболітів у традиційній медицині (традиційна медицина ), що також може бути біоактивацією рослинних компонентів [6]. Трави включали Cuscuta Chinensis Lam epithelium [7], Cassiae semen [8], Ephedra sinica Stapf [9], Melia to send Sieb.et Zucc.[10], Psoralea corylifolia Linn.[11], Gymura segetum(Lour)Merr [12], Leomurus aremisia (Laur)SY Hu F [13]. Polygonum multiflorum [14-16], Tripterygium Wilford Hook. f. [17,18], корінь Telfaria occidentalis [19,20] і так далі. У той же час люди звертали увагу на різні вікові групи, такі як немовлята [2], діти [21-23], дорослі [24], вагітність і післяпологовий період [13,25-27] у застосування засобів народної медицини. Рідкі китайські патентовані ліки, особливо для ін’єкцій, привернули більше уваги дослідників, як ін’єкції Xiyanping [28], пероральна рідина Tianfoshen [29] та ін’єкції пустирника [13]. Було застосовано нову технологію виявлення, таку як мультиспектральна оптико-акустична томографія (MSOT), яка відображає місце 1 точного ушкодження печінки, спричиненого фітотерапією, з 3D-інформацією неінвазивним способом за допомогою коефіцієнтометричного нанозонда на основі кон’югованого полімеру [14]. Підхід обчислювальної токсикології також застосовувався для скринінгу гепатотоксичних інгредієнтів у традиційній медицині [15]. Крім того, Китай відіграв ключову роль у сприянні стрімкому підйому в цій галузі. Статистичний аналіз щорічних публікацій токсикологічних досліджень традиційної медицини у відносних відсотках у різних країнах наведено на рисунку 1. США посіли другу важливу країну, тоді як Індія була приєднана до Канади, а Бразилія посіла третє місце в дослідженні токсикології традиційної медицини. Крім того, порівняно з 2018 роком, багато країн, як-от Австралія, Німеччина та Великобританія, почали звертати увагу на оцінку безпеки традиційної медицини.
Органна токсичність
Печінка вважається першим токсичним органом-мішенню в ТБ
Печінка є найважливішим органом метаболізму та детоксикації ліків в організмі. Оскільки ураження печінки, викликане травами, було зростаючою клінічною та економічною проблемою в усьому світі, у 2019 році було проведено велику кількість досліджень, присвячених токсичності печінки. Наприклад, нові технології виявлення, такі як MSOT, що дозволяють визначити точне місце розташування Fallopia multiflora (Thunb.)Harald- індуковане пошкодження печінки з 3D-інформацією було застосовано внаслідок окислювального/нітрозативного стресу, спричиненого гепатично генерованими активними формами кисню/активними формами азоту [14]. Для скринінгу гепатотоксичних інгредієнтів Fallopia multiflora(Thunb.)Harald було застосовано обчислювальний токсикологічний підхід [15]. Для розкриття механізму гепатотоксичності, спричиненої Melia toosendam Sieb.et Zucc., у мишей було використано об’єднання екзосомальних мікроРНК сироватки та мікроРНК печінки [10]. Тим часом метаболізм зазвичай використовувався для відображення холестатичного ураження печінки, спричиненого псораленом 30, ізопсораленом 30] і Gvura segetum (Louar :) [12], а також метаболічних розладів, таких як метаболізм гліцерофосфоліпідів, первинний біосинтез жовчних кислот, метаболізм сфінголіпідів, фенілаланін, тирозин і біосинтез триптофану та метаболізм тирозину Дафне генкан Зіб. et Zucc.[31]Ghycyrrhia uralensis Fisch.[31], Sophora flavescens Ait. [32] і Xysmalobium undulatum [33].
У традиційній медицині нирки вважаються другим токсичним органом-мішенню
Нирковий кровотік рясний, на нього припадає 25 відсотків серцевого викиду, тому велика кількість ліків може досягати нирки з потоком крові, щоб викликати патологічні зміни. Наприклад, аристолохієва кислота I раніше була визнана основною причиною нефропатії аристолохієвої кислоти [34]. Протягом 2019 року була використана нецільова метабономіка на основі рідинного хроматографа та мас-спектрометра, щоб виявити, що аристолохієва кислота I пригнічує метаболізм амінокислот, метаболізм глюкози, бета-окислення жирних кислот і цикл трикарбонових кислот у самців мишей [35]. Аристолохієва кислота I також може реагувати з геномною ДНК, утворюючи стійкі адукти ДНК з пуринами, що викликає нефротоксичність [36]. Хіміотерапія зазвичай викликає нефротоксичність, як і цисплатин [37| і доксорубіцин [38]. У 2019 році дослідники повідомили, що екстракт виноградних вичавок не захищає від нефротоксичності, спричиненої цисплатином, але підсилює токсичну дію цисплатину [37]. Dioscorea bulbifera L. затримувала виведення доксорубіцину та накопичувала доксорубіцин в організмі, що було пов’язано з пригніченням ним Р-глікопротеїну в печінці та нирках [38]. Крім того, повідомлялося, що пара несумісних трав Euphorbia kansui TNLiou ex SB Ho та Glycyrrhiza uralensis Fisch. індукував гепатотоксичність і нефротоксичність і послаблював ефект відвару Gansui Banxia [39].
Інші токсичні органи-мішені традиційної медицини
У 2019 році огляд запровадив отруєння токсичними рослинами в Гонконзі. Було виявлено 62 випадки, пов’язані з 26 видами отруйних рослин, серед яких Alocasia mycorrhizas (гігантська алоказія), Gelsemium elegans (витончений джесамін) і рододендрон (азалія) були трьома видами, які найчастіше зустрічалися. Шлунково-кишкова токсичність (n=30, 48 відсотків), неврологічна токсичність (n=22, 35 відсотків) і гепатотоксичність (n =6, 10 відсотків) були трьома найпоширенішими клінічними проблемами. Сорок дев'ять (79 відсотків) і вісім (13 відсотків) пацієнтів мали легку та помірну токсичність відповідно. Усі вони незабаром одужали завдяки підтримуючому лікуванню в традиційній медицині. Решта п'ять (8 відсотків) пацієнтів зазнали серйозної токсичності, що потребувало підтримки інтенсивної терапії [40].
Тим часом механізми репродуктивних ушкоджень, викликаних комбінацією Daphne genkwa Sieb. et Zucc. і Glycyrrhiza uralensis Fisch. [31], кардіотоксичність і нейротоксичність, викликана диефірними та моноефірними дитерпеноїдними алкалоїдами в обробленому Aconitum Carmichael Debx. корінь [41], кардіотоксичність, спричинену Chloranthus serratus [42], ураження шлунково-кишкового тракту, викликане Gardenia jasminoides Ellis [43], і так далі були пояснені в 2019 році. Ці екстракти слід використовувати з обережністю. Узагальнений статистичний аналіз щорічних публікацій, що стосуються різних токсичних органів-мішеней, спричинених традиційною медициною, підсумовано на малюнку 2.

Рисунок 1. Статистичний аналіз щорічних публікацій про токсикологічні дослідження народної медицини у відносних відсотках у різних країнах. Народна медицина
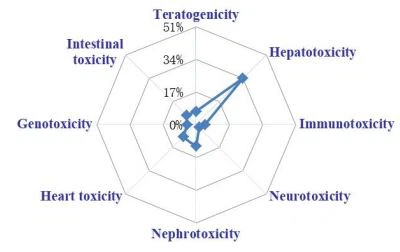
Малюнок 2. Статистичний аналіз щорічних публікацій про токсикологічні дослідження традиційної медицини за відносними відсотками щодо різних токсичних органів-мішеней. Народна медицина
Поточні досягнення
Ембріони рибок даніо популярні для оцінки безпеки традиційної медицини
Наразі оцінка безпеки застосована на клітинному, органному та індивідуальному рівнях. Гризуни розглядаються як загальні індивідуальні моделі для аналізу безпеки традиційної медицини або натуральних продуктів. Тим часом ембріони рибок даніо широко використовуються через їх швидкість, середню продуктивність і економічну ефективність. У 2019 році його використовували для оцінки захисту печінки та гепатотоксичності сайкосапоніну А [44], алое-емодіну [45] та триптоліду [46], тератогенності насіння та плодів Momordica charantia [47], серцевої токсичності тхора Libidibia ( juca) [48], репродуктивна токсичність Endopleura Uchi (Huber) Cuatrec [49] і так далі. Хоча Caenorhabditis elegans [50] і drosophila [51] нещодавно були популярними в оцінці безпеки різних хімічних сполук, у 2019 році не було відповідних досліджень у традиційній медицині.

Оцінка безпеки народної медицини для різних типів людей
Останнім часом безпека ліків була стурбована різними типами людей, такими як немовлята [2], діти [21–23], дорослі [24] і матері [13, 25–27]. У 2019 році в огляді повідомлено про безпеку лікарського засобу рослинного походження під час вагітності та в післяпологовий період [25]. У цьому звіті мигдальна олія може спровокувати передчасні пологи, вживання орального листя малини було пов’язане з кесаревим розтином; застосування інтенсивного вживання солодки було відносно ранніх передчасних пологів у 3.07-рази. Повідомлялося також, що африканська фітотерапія мванафепо пов’язана з материнською захворюваністю, смертю новонароджених або захворюваністю [25]. Тим часом інші дослідники повідомили, що водний екстракт Anastatica hierochuntica [26] і снюс тютюну [27] демонстрували потенційну токсичність під час вагітності. Більше того, він привернув увагу до оцінки безпеки токсичних металів у широко використовуваних фармацевтичних рослинних продуктах на ринку Йорданії [2], змішаному екстракті, що містить корінь алтея, квіти ромашки, траву хвоща, листя волоського горіха, траву деревію, кору дуба та трава кульбаби в області народної медицини гострого небактеріального тонзиліту [21], а також зелений чай [22] у дітей.
Нова технологія дослідження токсикології
У 2019 році була використана нова технологія в токсикологічній оцінці. Наприклад, підхід обчислювальної токсикології також застосовувався для скринінгу гепатотоксичних інгредієнтів у традиційній медицині [15]. Для швидкої ідентифікації рослинних токсинів використовували електророзпилювальну лазерну десорбційну іонізаційну мас-спектрометрію [1]. Зображення MSOT у поєднанні з полімерним полімерним нанозондом було застосовано для точного визначення місця пошкодження печінки, спричиненого традиційною медициною, з 3D-інформацією неінвазивним способом [14]. Крім того, інтеграція екзосомальних мікроРНК сироватки та профілів мікроРНК печінки була використана для розкриття механізму індукованої традиційною медициною гепатотоксичності у мишей [10].
Висновок
У сукупності щорічні дослідження показують, що печінка, нирки та серце є основними токсичними органами-мішенями традиційної медицини. Їх токсичні механізми включають апоптоз клітин, порушення метаболізму, окислювальний стрес, запальне пошкодження, фіброз печінки та нирок і навіть індукцію канцерогенезу. Безпека ліків традиційної медицини хвилювала різних людей, наприклад немовлят. дітей і матері. Крім гризунів, ембріони рибок даніо вважалися звичайними моделями для оцінки безпеки традиційної медицини. Нові технології в токсикології зосереджені на тому, як відстежувати та ідентифікувати токсини в традиційній медицині, як відображати точне місце пошкодження тканини, спричиненого традиційною медициною, за допомогою 3D-інформації та як пояснити механізм токсичності, спричиненої традиційною медициною. У майбутньому дослідження механізму токсичності інших органів-мішеней, безпеки ліків у людей похилого віку, нові моделі та методи повинні бути використані в профілактиці токсикології традиційної медицини.

Список літератури
1 Su H, Liu KT, Chen BH та ін. Швидка ідентифікація рослинних токсинів за допомогою електророзпилювальної лазерної десорбційної іонізаційної мас-спектрометрії для невідкладної допомоги. J Food Drug Anal 2019, 27: 415–427.
2. Альхусбан А.А., Ата С.А., Шраїм С.А. Оцінка безпеки токсичних металів у широко використовуваних фармацевтичних рослинних продуктах і традиційних травах для немовлят на ринку Йорданії. Biol Trace Elem Res 2019, 187: 307–315.
3. Офусорі А.Е., Мудлі Р., Йонналагадда С.Б. Поширення елементів у їстівному листі Celosia original із західних і північних регіонів Нігерії. J Environ Sci Health B 2019, 54: 61–69.
4. Сова-Рогозінська Н., Сомінка Х., Новаковська-Голацька Дж. та ін. Внутрішньоклітинний транспорт і цитотоксичність білкового токсину рицину. Токсини (Базель) 2019, 11: 350.
5. Ling C, Zhang Y, Li J та ін. Клінічне використання токсичних білків і пептидів з Tian Hua Fen і отрути скорпіона. Curr Protein Pept Sci 2019, 20: 285–295.
6. Wen B, Gorecki P. Біоактивація рослинних компонентів: механізми та токсикологічна значимість. Drug Metab Rev 2019, 51: 453–497.
7. Чабра А, Мораді Т, Азадбахт М та ін. Етнофармакологія епітелію Cuscuta: комплексний огляд етноботаніки, фітохімії, фармакології та токсичності. J Ethnopharmacol 2019, 231: 555–569.
8. Yang JL, Zhu A, Xiao S та ін. Антрахінони у водному екстракті сперми Cassiae викликають ураження печінки у щурів через порушення ліпідного обміну. Фітомедицина 2019, 64: 153059.
9. Odaguchi H, Hyuga S, Sekine M та ін. Побічні ефекти трави ефедри та безпека екстракту трави ефедри без алкалоїдів ефедрину (EFE). Yakugaku Zasshi 2019, 139: 1417–1425.
10. Yu LQ, Zheng J, Li JY та ін. Інтеграція екзосомальних мікроРНК сироватки та профілів мікроРНК печінки розкриває функціональну роль аутофагії та механізми індукованої Fructus Meliae Toosendan гепатотоксичності у мишей. Biomed Pharmacother 2020, 123: 109709.
11. Wang Y, Zhang H, Jiang JM та ін. Мультиорганна токсичність, викликана EtOH екстрактом Fructus Psoraleae у щурів Wistar. Фітомедицина 2019, 58: 152874.
12. Xiong A, Shao Y, Fang L та ін. Порівняльний аналіз токсичних компонентів у різних лікарських частинах Gynura japonica та оцінка його токсичності на мишах. Фітомедицина 2019, 54: 77–88.
13. Meng W, Li R, Zha N та ін. Ефективність і безпека додаткової терапії пустирником до карбопросту трометаміну для профілактики післяпологової втрати крові: мета-аналіз рандомізованих контрольованих досліджень. J Obstet Gynaecol Res 2019, 45: 47 56.
14. Wu Y, Sun L, Zeng F та ін. Раціонометричний нанозонд на основі кон’югованого полімеру для оцінки in vivo гепатотоксичності, викликаної фітотерапією, за допомогою візуалізації MSOT. Фотоакустика 2019, 13: 6–17.
15. He S, Zhang X, Lu S та ін. Обчислювальний токсикологічний підхід для скринінгу гепатотоксичних інгредієнтів у традиційних китайських ліках: Polygonum multiflorum Thunb як приклад. Біомолекули 2019, 9: 577.
16. Byeon JH, Kil JH, Ahn YC та ін. Систематичний огляд опублікованих даних про пошкодження печінки, спричинене травами. J Ethnopharmacol 2019, 233: 190–196.
17. Wang JM, Li JY, Cai H та ін. Nrf2 бере участь у механізмах зниження токсичності та посилення протипухлинного ефекту Radix Tripterygium wilfordii на S180-мишах за допомогою технології обробки трав. Pharm Biol 2019, 57: 437–448.
18. Wang XW, Tian RM, Yang YQ та ін. Триптріолід протидіє індукованому триптолідом апоптозу нефроцитів шляхом інгібування окисного стресу in vitro та in vivo. Biomed Pharmacother 2019, 118: 109232.
19. Ogunmoyole T, Oladele FC, Aderibigbe A та ін. Гепатотоксичність екстрактів коренів Telfaria occidentalis на щурах-альбіносах Wistar. Heliyon 2019, 5: e01617.
20. Guo Y, Xiao D, Yang X та ін. Пренатальний вплив алкалоїдів піролізидину викликав гепатотоксичність і легеневе ураження у плодів щурів. Reprod Toxicol 2019, 85: 34–41.
21. Попович В, Кошель І, Малофійчук А та ін. Рандомізоване відкрите багатоцентрове порівняльне дослідження терапевтичної ефективності, безпеки та переносимості екстракту BNO 1030, що містить корінь алтея, квітки ромашки, траву хвоща польового, волоський горіх
листя, трава деревію, кора дуба, трава кульбаби в області народної медицини гострого небактеріального тонзиліту у дітей віком від 6 до 18 років. Am J Otolaryngol 2019, 40: 265–273.
22. D'Agostinoa D, Cavalieri ML, Arcucci MS. Важкий гепатит, викликаний інтоксикацією дитини зеленим чаєм. Звіт про випадок. Arch Argent Pediatr 2019, 117: e655–e658.
23. Mazhar H, Foster BC, Neck C та ін. Оцінка причинно-наслідкового зв’язку між природним продуктом для здоров’я та лікарським засобом у педіатричних звітах про несприятливі події, пов’язані з прийомом ліків від синдрому дефіциту уваги/гіперактивності. J Child Adolesc Psychopharmacol 2019.
24. Fu B, Zhai X, Xi S та ін. Оцінка безпеки нової традиційної китайської медичної суміші, формули Ciji-Hua'ai-Baosheng II, на моделях дорослих гризунів. Evid Based Complement Alternat Med 2019, 2019: 3659890.
25. Munoz Balbontin Y, Stewart D, Shetty A та ін. Застосування лікарських засобів рослинного походження під час вагітності та в післяпологовому періоді: систематичний огляд. Obstet Gynecol 2019, 133: 920–932.
26. Md Zin SR, Kassim NM, Mohamed Z та ін. Потенційні токсичні ефекти водного екстракту Anastatica hierochuntica на внутрішньоутробний розвиток щурів Sprague-Dawley. J Ethnopharmacol 2019, 245: 112180.
27. Martinez IKC, Sparks NRL, Madrid JV, et al. Відео кінетичний аналіз кальцифікації в культурах живих остеогенних ембріональних стовбурових клітин людини показує токсичну дію екстракту тютюну Снус на розвиток. Toxicol Appl Pharmacol 2019, 363: 111–121.
28. Zheng R, Tao L, Kwong JSW та ін. Фактори ризику, пов'язані з тяжкістю побічних реакцій на лікарський засіб при ін'єкції Xiyanping: відповідний аналіз схильності. J Ethnopharmacol 2020, 250: 112424.
29. Zhao L, Wang J, Li H та ін. Безпека та ефективність пероральної рідини Tianfoshen у пацієнтів з недрібноклітинним раком легенів як допоміжна терапія. Evid Based Complement Alternat Med 2019, 2019: 1375439.
30. Wang Y, Zhang H, Jiang JM та ін. Гепатотоксичність, спричинена псораленом та ізопсораленом із Fructus Psoraleae: щури Вістар більш вразливі, ніж миші ICR. Food Chem Toxicol 2019, 125: 133–140.
31. Chen YY, Tang YP, Shang EX та ін. Оцінка несумісності Genkwa Flos і Glycyrrhizae Radix et Rhizoma з біохімічним, гістопатологічним і метабономічним підходом. J Ethnopharmacol 2019, 229: 222–232.
32. Jiang P, Sun Y, Cheng N. Метаболомічна характеристика печінки гепатотоксичності, спричиненої спиртовим екстрактом Sophora flavescens, у щурів за допомогою мас-спектрометрії UPLC/LTQ-Orbitrap. Ксенобіотика 2019: 1–7.
33. Zhao C, Jia Z, Li E та ін. Оцінка гепатотоксичності Euphorbia kansui на личинках даніо in vivo. Фітомедицина 2019, 62: 152959.
34. Zhang HM, Zhao XH, Sun ZH та ін. Визнання токсичності аристолохієвої кислоти. J Clin Pharm Ther 2019, 44: 157–162.
35. Cui Y, Han J, Ren J та ін. Нецільова метабономіка на основі РХ-МС виявила, що аристолохієва кислота I індукує тестикулярну токсичність шляхом інгібування метаболізму амінокислот, метаболізму глюкози, бета-окислення жирних кислот і циклу ТСА у самців мишей. Toxicol Appl Pharmacol 2019, 373: 26–38.
36. Bastek H, Zubel T, Stemmer K та ін. Порівняння рівнів аддукту ДНК, отриманого з аристолохієвої кислоти I, у моделях ниркової токсичності людини. Токсикологія 2019, 420: 29–38.
37. Neag MA, Mitre CI, Mitre AO та ін. Парадоксальний ефект екстракту виноградних вичавок на викликане цисплатином гостре ураження нирок у щурів. Фармацевтика 2019, 11: 656.
38. Qu X, Zhai J, Hu T та ін. Dioscorea bulbifera L. затримує виведення доксорубіцину та посилює спричинену доксорубіцином кардіотоксичність і нефротоксичність шляхом пригнічення експресії Р-глікопротеїну в печінці та нирках мишей. Ксенобіотика 2019, 49: 1116–1125.
39. Cui Y, Wang R, Zhang Y та ін. Дослідження механізму гепатотоксичності та нефротоксичності, спричиненої несумісною парою трав Gansui-Gancao, і ослабленого ефекту відвару Gansui Banxia за допомогою UHPLC-FT-ICR-MS метабономічного аналізу плазми. J Pharm Biomed Anal 2019, 173: 176–182.
40. Ng WY, Hung LY, Lam YH та ін. Отруєння токсичними рослинами в Гонконгу: огляд за 15- рік. Hong Kong Med J 2019, 25: 102–112.
41. Zhang M, Peng Y, Wang M та ін. Вплив сумісності відвару Si-Ni з метаболізмом у кишкових бактеріях на транспортування токсичних дитерпеноїдних алкалоїдів із обробленого кореня аконіту через моношари Caco-2. J Етнофармакол
2019, 228: 164–178.
42. Sun SP, Li HX, Zhang XP та ін. Механізми токсичності та кардіотоксичності спиртового екстракту кореня, стебла та листя Chloranthus serratus. Fa Yi Xue Za Zhi 2019, 35: 224–229. (китайська)
43. Zhou J, Yao N, Wang S та ін. Пошкодження шлунково-кишкового тракту, спричинене Fructus Gardeniae, було пов’язане із запальною відповіддю, опосередкованою порушенням метаболізму вітаміну B6, фенілаланіну, арахідонової кислоти, таурину та гіпотаурину. J Ethnopharmacol 2019, 235: 47–55.
44. Xia Q, Han LW, Zhang Y та ін. Дослідження захисту печінки та гепатотоксичності сайкосапоніну на моделі рибки даніо. Zhongguo Zhong Yao Za Zhi 2019, 44: 2662–2666. (китайська)
45. Quan Y, Gong L, He J та ін. Алое-емодін індукує гепатотоксичність шляхом активації запального шляху NF-kappaB і шляху апоптозу P53 у рибок даніо. Toxicol Lett 2019, 306: 66–79.
46. Huo J, Yu Q, Zhang Y та ін. Триптолід-індукована гепатотоксичність через апоптоз і аутофагію у рибок даніо. J Appl Toxicol 2019, 39: 1532–1540.
47 Хан М.Ф., Абута Н., Наср Ф.А. та ін. Гіркий гарбуз (Momordica charantia) має токсичний вплив на розвиток, як виявлено під час скринінгу насіння та екстрактів плодів ембріонів рибок даніо. BMC Complement Altern Med 2019, 19: 184.
