Трансплантація нирки: імуносупресія після трансплантації
Mar 15, 2022
Контакт: Одрі Ху Whatsapp/hp: 0086 13880143964 Електронна пошта:audrey.hu@wecistanche.com
ЧАСТИНА Ⅱ: Цукровий діабет після трансплантації та вибір імуносупресії у пацієнтів похилого віку та пацієнтів із ожирінням
Девід А та Аксельрод та ін.
Обґрунтування та мета: Посттрансплантаціяцукровий діабет (ЦД) післятрансплантація ниркипідвищує захворюваність і смертність, особливо у пацієнтів похилого віку та пацієнтів із ожирінням. Ми мали на меті вивчити впливімуносупресіявідбір на ризикпосттрансплантаційнийЦД як серед людей похилого віку, так і серед хворих на ожирінняпересадка ниркиодержувачі.
Вивчати дизайн:Ретроспективне дослідження бази даних. Налаштування й учасники: реципієнти лише трансплантації нирки віком понад 18 років із 2005 по 2016 рік у Сполучених Штатах із записів US Renal Data System, які об’єднують записи Organ Procurement and Transplantation Network/United Network for Organ Sharing із вимогами про оплату Medicare . Експозиції: різніімуносупресіясхем у перші 3 місяці після трансплантації.
результати: Development of DM >Від 3 місяців до -1 року після трансплантації.
Аналітичний підхід:Ми використали багатофакторну регресію Кокса для порівняння захворюваностіпосттрансплантаційнийDM відімуносупресіярежим з еталонною схемою тиреоглобуліну (TMG) або алемтузумабу (ALEM) з такролімусом плюс мікофенолова кислота плюс преднізон із використанням оберненого зважування схильності.
Результати:12,7 відсоткапересадка ниркиреципієнти розвинпосттрансплантаційнийЦД з вищою частотою випадків у літніх (255 років проти<55 years:16.7%="" vs="" 10.1%)and="" obese="" (body="" mass="" index="" [bml]≥30="" kg/m²="" vs=""><30 kg/m∶17.1%="" vs="" 10.9%)pa-tients.="" the="" incidence="" of="">посттрансплантаційнийDM був нижчим при уникненні стероїдів [TMG/ALEM плюс відсутність преднізону (8,4 відсотка) та IL2rAb плюс відсутність преднізону (9,7 відсотка)], ніж TMG/ALEM при потрійній терапії (13,1 відсотка). Після коригування характеристик донора та реципієнта TMG/ALEM з уникненням стероїдів було корисно для всіх груп [вік < 55="" років:="" скоригована="" чсс="" (ahr),="" 0.63="" (95-відсотковий="" довірчий="" інтервал="" [cl],="" 0.54-0.72)="" ;="" вік="" більше="" або="" дорівнює="" 55="" рокам:="" ahr,="" 0.69="" (95="" відсотків="" cl="" 0.60-0.79;=""><30 kg/m²∶ahr,0.69="" (95%cl,="" 0.60-0.78);="" bmi≥="" 30="" kg/m²∶="" ahr,0.67="" (95%cl,="" 0.57-0.79)].="" however,="" il2rab="" with="" steroid="" avoidance="" was="" beneficial="" only="" for="" older="" patients="" (ahr,="" 0.76;="" 95%="" cl,="" 0.58-0.99)="" and="" for="" those="" with=""><30 kg/m²(ahr,="" 0.63;95%="" cl,="">
Обмеження:Ретроспективне дослідження та брак даних проімуносупресіярівнях.
Висновки:Сприятливий вплив уникнення стероїдів за допомогою такролімусупосттрансплантаційнийСхоже, що ЦД залежить від віку пацієнта та режиму індукції.
Користь цистанче: живить нирки та лікує ниркизахворювання
НАТИСНІТЬ ТУТ, ЩОБ ЧАСТИНА Ⅰ
РЕЗУЛЬТАТИ
Клінічна характеристика
Серед 193 984пересадка ниркиреципієнтів у період дослідження 40108 мали страховку Medicare на момент трансплантації та не мали діабету до трансплантації. Порівняно із загальною популяцією трансплантологів, вибірка допомоги Medicare без діабету відрізнялася за віком, расою, статусом зайнятості, ІМТ та причиною термінальної стадії захворювання нирок (таблиця 1), що відповідає попереднім звітам. Серед вибірки 38,0% отримувачів були старші або дорівнювали 55 рокам, 58,8% були чоловіками, 30,2% були афроамериканцями, а 27,5% мали ІМТ більше або дорівнювали 30 кг/м2. TMG/ALEM плюс потрійна терапія була найпоширенішоюімуносупресіярежим (47,2 відсотка), потім TMG/ALEM без преднізону (20.0 відсотка), IL2rAb плюс потрійна терапія (16,0 відсотка), схеми на основі CsA (5,6 відсотка) та mTORi схем лікування (5,7%). IL2rAb плюс відсутність преднізону (2,2 відсотка) і такролімус або такролімус плюс преднізон з будь-якою індукцією (3,3 відсотка) зазвичай не використовувалися. Розподіл клінічних характеристикпересадка ниркиодержувачі були різнимиімуносупресіярежими (табл. 1).
Частота та ризик посттрансплантаційного ЦД
Серед різногоімуносупресіяRegimens: Older Versus Younger The incidence of DM >Від 3 місяців до -1 року після трансплантації було значно вищим серед літніх людей у вибірці (вік більше або дорівнює 55 рокам, 16,7 відсотка проти<55 years,="" 10.1%;="" p="" <="" 0.001).="" among="" older="" patients,="" the="" incidence="" of="">посттрансплантаційнийЦД протягом 12 місяців відрізнявся більш ніж у 2{2}}рази між схемами: від 11,6 відсотка серед пацієнтів, які отримували TMG/ALEM без преднізону, до 26,3 відсотка серед пацієнтів, які отримували схеми на основі mTORi (рис. 1A). Серед пацієнтів молодшого віку захворюваність напосттрансплантаційнийDM коливався від 6,1 відсотка (IL2rAb плюс відсутність преднізону) до 20,2 відсотка (mTORi).
Після поправки на потенційні суперечливі відмінності через клінічні характеристики, ризикипосттрансплантаційнийСД значно відрізнявся між схемами (рис. 2A). Серед літніх реципієнтів ризикпосттрансплантаційнийDM був зменшений у тих, хто отримував TMG/ALEM без преднізону [скоригований коефіцієнт ризику (aHR), {{0}}.69; 95% ДІ, 0.60-0.79] або з IL2rAb без преднізону (aHR, 0.76; 95% ДІ, 0.58-0.99), тоді як ризики були вищими при терапії на основі mTORi та схемах на основі CsA, ніж при TMG/ALEM плюс потрійна терапія. Вплив mTORiімуносупресіяна ризикпосттрансплантаційнийЦД змінювався залежно від віку [вік більше або дорівнює 55 рокам: aHR, 1,69 (95% ДІ, 1.46- 1.96); вік < 55="" років:="" ahr,="" 1,24="" (95%="" ді,="" 1.03-1.49);="" взаємодія="" за="" віком="" p="0.002]." серед="" молодших="" пацієнтів="" лише="" tmg/alem="" плюс="" відсутність="" преднізону="" асоціювалися="" з="" меншим="">посттрансплантаційнийСД (aHR, {{0}}.63; 95 відсотків ДІ, 0.54- 0.72). Не було статистично значущої користі від IL2rAb плюс відсутність режиму преднізону у молодших пацієнтів.

Фігура 1.Differential incidences of DM >3 місяці--1 рік після трансплантації середпересадка ниркипацієнтів згідноімуносупресіярежим на основі (A) віку на момент трансплантації та (B) ІМТ на момент трансплантації. Потрійна терапія складалася з Tac плюс MPA/AZA плюс Pred. Скорочення: АЛЕМ, алемтузумаб; АЗА, азатіоприн; ІМТ, індекс маси тіла; CsA, циклоспорин А; ЦД, цукровий діабет; IL2rAb, антитіло до рецептора інтерлейкіну-2; ISx,імуносупресія; MPA, мікофенолова кислота; mTORi, мішень інгібітора рапаміцину у ссавців; Пред, преднізон; Так, такролімус; ТМГ, тиреоглобулін.
Вплив ожиріння на ризики посттрансплантаційного ЦД серед різних схем імуносупресії
Пацієнти з ожирінням мали значно більший ризикпосттрансплантаційнийД.М., незалежно відімуносупресія regimen (BMI < 30 kg/m2: 10.9%, BMI ≥ 30 kg/m2: 17.1%; P < 0.0001). Obese patients treated with mTORi-based regimens had the highest incidence of DM >Від 3 місяців до - 1-року після трансплантації (32,4 відсотка), тоді як у пацієнтів без ожиріння, які приймали такролімус або такролімус плюс преднізон, було найнижче (7,1 відсотка; рис. 1B). Застосування TMG/ALEM плюс відсутність преднізону зменшило ризикпосттрансплантаційнийЦД у пацієнтів з ІМТ більше або дорівнює 30 кг/м2 до 11,5 відсотка, тоді як у 16,0 відсотка пацієнтів, які отримували IL2rAb без преднізону, розвинувсяпосттрансплантаційнийDM.
Після поправки на змішування, уникнення стероїдів з індукцією TMG/ALEM зменшило ризикпосттрансплантаційнийЦД у пацієнтів із ожирінням (aHR, {{0}}.67; 95% ДІ, 0.57-0.76; рис. 2B). Навпаки, уникання стероїдів із індукцією IL2rAb призводило до ризику розвитку цукрового діабету після трансплантації, еквівалентного ризику пацієнтів із ожирінням, які отримували потрійну терапію (aHR, 0.99; 95% ДІ, 0.66-1.49). РизикпосттрансплантаційнийСД при терапії на основі mTORi був значно більшим, ніж при потрійній терапії (aHR, 1,40; 95% ДІ, 1.12-1.75). Серед пацієнтів без ожиріння обидва режими уникнення стероїдів були пов’язані з нижчими показникамипосттрансплантаційнийDM [TMG/ALEM плюс без преднізону: aHR, {{0}}.69 (95 відсотків ДІ, 0.{60-0.78); IL2rAb: aHR, 0.63 (95% ДІ, 0.46-0.87)], тоді як використання mTORi підвищує ризик (aHR, 1,22; 95% ДІ, 1.04-1 .44).
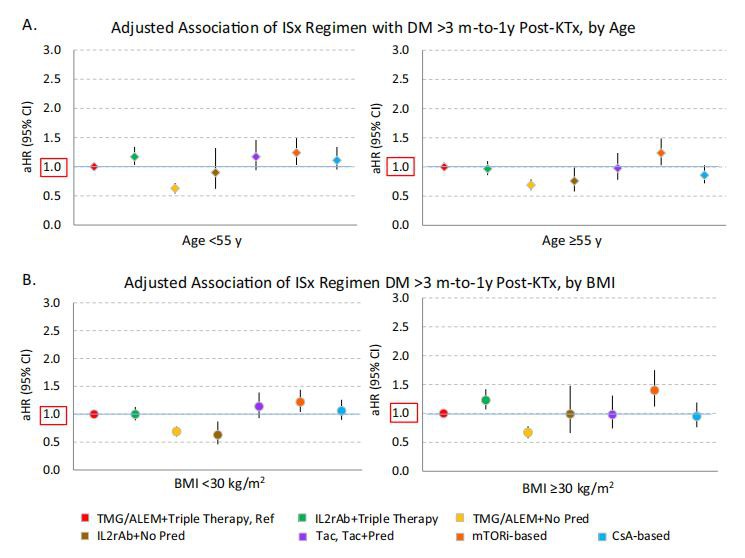
малюнок 2. Adjusted risks of DM >Від 3 місяців до -1 років після трансплантації серед пацієнтів, які отримували різніімуносупресіясхеми на основі (А) віку на момент трансплантації та (В) ІМТ на момент трансплантації. Потрійна терапія складалася з Tac плюс мікофенолової кислоти/азатіоприну плюс Pred. Скорочення: AHR, скоригований коефіцієнт ризику; АЛЕМ, алемтузумаб; ІМТ, індекс маси тіла; CsA, циклоспорин А; ДІ, довірчий інтервал; ЦД, цукровий діабет; IL2rAb, антитіло до рецептора інтерлейкіну-2; ISx,імуносупресія; mTORi, мішень інгібітора рапаміцину у ссавців; Пред, преднізон; Так, такролімус; ТМГ, тиреоглобулін.

ДИСКУСІЯ
Це дослідження великої сучасної вибіркипересадка ниркипацієнтів підтверджує загальну користь від кортикостероїдзберігаючих схем серед пацієнтів із ризикомпосттрансплантаційнийЦД, включаючи пацієнтів старшого віку або з вищим ІМТ, після коригування супутніх захворювань (наприклад, гепатиту С) і характеристик пацієнта (наприклад, расової/етнічної приналежності). Хоча поточні опубліковані рекомендації свідчать про цеімуносупресіясхеми повинні бути обрані для забезпечення «найкращих імунологічних результатів» для пацієнтів, незалежно відпосттрансплантаційнийРизик цукрового діабету, ця рекомендація не враховує відмінності впересадка ниркиризики та переваги для одержувачів.5,44 Попередні дослідження, які оцінювали ризикипосттрансплантаційнийДМ середпересадка ниркиреципієнтів з різнімуносупресіясхеми не були оновлені поточною підтримуючою терапією на основі такролімусу та ефективною індукцією.
Пацієнти похилого віку (віком понад 55 років) мають підвищений ризикпосттрансплантаційнийЦД і, здається, оптимально лікуються за допомогою режиму без стероїдів, що супроводжується відповідною індукцією (або TMG/ALEM, або IL-2rAb). Літні пацієнти після трансплантації піддаються більшому ризику неінфекційних ускладнень і мають меншу ймовірність відторгнення після трансплантації внаслідок імунодефіциту.22-26,37,39-43,50 Останні дані аналізу реєстру трансплантатів показали запропонував потенційні переваги нижчої інтенсивності для виживання пацієнта та трансплантатаімуносупресіясхеми (наприклад, стероїдозберігаючі схеми) для літніхпересадка нирки50 І навпаки, молодші пацієнти та пацієнти з ожирінням отримують переваги від схем уникнення стероїдів, але лише якщо компенсуючий ризик відторгнення зменшується за допомогою терапії, що виснажує Т-клітини (TMG/ALEM).
Існують суперечливі дані щодо довгострокових переваг відміни стероїдів у порівнянні з довгостроковим лікуванням низькими дозами кортикостероїдів щодо ризикупосттрансплантаційнийDM.41,42 Хоча відміна 10 мг преднізону на добу була пов’язана зі зниженням резистентності до інсуліну, є менша впевненість щодо користі від його усунення впересадка ниркиреципієнти, які отримують нижчі дози преднізону, такі як 5 мг на день.58,59 У попередньому звіті було припущено, що чутливість до інсуліну покращилася при зменшенні дози преднізону з 10 мг/день до 5 мг/день, але не було додаткового покращення після відміни від дози 5- мг.59 Клінічні дані про переваги протоколів уникнення стероїдів змінювалися, оскільки підтримуючі схеми переходили з CsA на такролімус. У дослідженні HARMONY, у якому порівнювали режими індукції у пацієнтів, які отримували такролімус плюс мікофенолову кислоту, швидка відміна кортикостероїдів була пов’язана з меншою частотоюпосттрансплантаційнийСД без збільшення ризику відторгнення.60 У попередніх дослідженнях є обмежені дані щодо ефекту уникнення/відміни стероїдів серед літніх реципієнтів із ожирінням.41,42,61-64 Нещодавнє дослідження наукового реєстру реципієнтів трансплантації (SRTR). з 44 635 першихпересадка ниркиt реципієнтів з ІМТ більше або дорівнює 30 кг/м2 також показали, що реципієнти з безпреднізономімуносупресіямали значно кращі результати, включаючи виживання пацієнта та трансплантата, порівняно з реципієнтами на підтримціімуносупресіяз преднізоном.65 У цьому дослідженні продовження будь-якої схеми преднізону було пов’язано з вищими показникамипосттрансплантаційнийЦД у пацієнтів як з низьким, так і з високим ризиком.
Загальновідомо, що CNI збільшують ризик гіперглікемії, оскільки вони порушують чутливість до інсуліну, зменшують вивільнення інсуліну та безпосередньо пошкоджують острівці підшлункової залози.22-26,66 Тому мінімізація або уникнення CNI як стратегія зниження ризику зпосттрансплантаційнийБуло оцінено DM.67 Рандомізоване контрольоване дослідження DIRECT підтвердило підвищену діабетогенність такролімусу порівняно з CsA серед реципієнтівпересадка нирки.68,69 Однак у цьому дослідженні використовували мінімальні рівні такролімусу, які були набагато вищими, ніж ті, які використовуються в поточній практиці. Зворотний розвиток діабету після заміни такролімусу на CsA впересадка ниркихворих напосттрансплантаційнийПовідомлялося про цукровий діабет.70 Таким чином, було запропоновано перехід з такролімусу на CsA для покращення метаболізму глюкози в реципієнтів трансплантації.71 Однак такролімус краще запобігає гострому відторгненню, і повідомлялося про збільшення епізодів відторгнення після переходу з такролімусу на CsA. , що ймовірно призведе до відновлення хронічної стероїдної терапії.40,72 Поточне дослідження не підтвердило зниження ризикупосттрансплантаційнийЦД у схемах на основі CsA de novo порівняно зі схемами на основі такролімусу з уникненням стероїдів. Можливо, що діабетогенний ефект такролімусу є дозозалежним, а мінімальні рівні такролімусу, які використовувалися в клінічній практиці у літніх реципієнтів, були не такими високими, як у молодих реципієнтів, що пояснює, чому порівнянний ризикпосттрансплантаційнийЦД спостерігався при порівнянні зі схемами на основі CsA в цій популяції.73 Крім того, нечасте використання CsA може обмежити статистичну потужність у цьому аналізі підгруп. Крім того, діабетогенні ефекти такролімусу, ймовірно, посилюються при одночасному застосуванні стероїдів. Таким чином, порівняно з такролімусом і CsA в схемах потрійної терапії не було значної користі для обох CNI. За відсутності стероїдів кращий захист такролімусу від відторгнення може зменшити частотупосттрансплантаційнийЦД шляхом обмеження використання високих доз стероїдів для відторгнення. Важливо зазначити, що враховуючи відносно рідкісне використання CsA на національному рівні, схема CsA в нашому дослідженні включала як пацієнтів, які отримували стероїди, так і пацієнтів із потрійною терапією. Однак, враховуючи високі показники відторгнення у пацієнтів із CsA без преднізону, рутинне збереження преднізону навряд чи буде використовуватися часто; таким чином, включення агрегованих пацієнтів з CsA є доречним.

Використання de novo схем на основі mTORi загалом виявилося гіршим, ніж підтримуюча терапія такролімусом, враховуючи підвищений ризик відторгнення. Попереднє дослідження даних Системи даних про нирки США також показало, що використання сиролімусу пов’язане з підвищеним ризикомпосттрансплантаційнийЦД, ймовірно, через вплив тривалого застосування преднізону в цій популяції.39 ЧастотапосттрансплантаційнийСД був вищим при застосуванні сиролімусу (у поєднанні з мікофенолату мофетилу або CNI), ніж при застосуванні CNI та мікофенолату мофетилу окремо.39 І навпаки, у дослідженні Symphony, у якому використовувалися нижчі цільові рівні сиролімусу (3 та 7 нг/мл), у реципієнтів mTORi розвинувсяпосттрансплантаційнийЦД із рівнем захворюваності серед пацієнтів, які отримували CsA та такролімус.40 Крім того, як зниження чутливості до інсуліну, так і послаблення компенсаторної відповіді на інсулін зберігаються, коли реципієнти переходять з CsA або такролімусу на сиролімус, що свідчить про те, що використання mTORi одних тільки режимів недостатньо, щоб повернути назад гіпометаболізм у реципієнтів трансплантації.74 Середпересадка ниркипацієнтів, наше дослідження також встановило, що схема на основі mTORi не забезпечувала переваг проти ризику ЦД після трансплантації. Враховуючи те, що ретроспективні дослідження виявили зв’язок схем на основі mTORi з підвищеним ризиком смертності, особливо у літніхпересадка ниркиреципієнтів, використання цих схем для уникнення такролімусу не є корисним.50,75
Це дослідження на основі реєстру має обмеження. По-перше, виходячи з характеру бази даних, дані проімуносупресіярівні, включаючи мінімальні рівні CNI та/або mTORi, та інші лабораторні дані були недоступні. Дані свідчать про те, що вплив такролімусу на ризикпосттрансплантаційнийЦД є дозозалежним і вираженим у реципієнтів з гіпертригліцеридемією та інсулінорезистентністю в анамнезі.73,76 По-друге, вибірімуносупресіяна схему могли вплинути невраховані в базі даних фактори ризику, такі як попередні епізоди відмови; характеристики донора; непереносимість стандартних ліків, в тому числі гематологічні відхилення; злоякісні новоутворення в анамнезі; або неможливість придбати ці ліки. Реципієнти з високим ризиком посттрансплантаційного ЦД, можливо, були переведені на CsA запобіжно, штучно збільшуючи ризик посттрансплантаційного ЦД у цій групі. Нарешті, захворюваністьпосттрансплантаційнийЦД у нашому дослідженні становив 12,7 відсотка протягом першого року, що дещо нижче, ніж у попередніх звітах, заснованих на оглядах клінічних записів.7-9 Пероральний тест на толерантність до глюкози є кращим тестом для діагностикипосттрансплантаційнийDM, але результати цього тесту недоступні в претензіях Medicare або даних OPTN.44 Можливо, щопосттрансплантаційнийЦМ було занижено, коли було встановлено з кодів діагнозу Medicare, але немає підстав вважати, що заниження відрізняєтьсяімуносупресіярежим. Отже, висновки, представлені в цій статті, мають бути дійсними та ґрунтуватися на дослідженні однієї з найбільших вибірок старших реципієнтів трансплантації, обстежених на цей результат на сьогоднішній день.
Підсумовуючи, серед застрахованих Medicareпересадка ниркиреципієнти, без стероїдівімуносупресіяасоціюється з меншим ризикомпосттрансплантаційнийDM. Ця перевага була підтверджена для пацієнтів із високим ризиком (старші люди; ІМТ більше або дорівнює 30 кг/м); однак важливість супутнього виснаження клітин була різною. Ці дані підтверджують врахування ризику неімунних ускладнень разом із ризиком відторгнення при виборіімуносупресіярежими впересадка ниркиреципієнтів, щоб мінімізувати захворюваність пацієнтівімуносупресія-супутні побічні ефекти.

СПИСОК ЛІТЕРАТУРИ
Jenssen T, Hartmann A. Цукровий діабет після трансплантації у пацієнтів із трансплантацією твердих органів. Nat Rev Endocrinol. 2019;15(3):172-188.
Хеккінг М., Шаріф А., Еллер К., Дженссен Т. Лікування діабету після трансплантації:імуносупресія, рання профілактика та нові протидіабетичні засоби. Transpl Int. 2021;34(1):27-48.
Shivaswamy V, Boerner B, Larsen J. Цукровий діабет після трансплантації: причини, лікування та вплив на результати. Endocr Rev. 2016;37(1):37-61
Sharif A, Cohney S. Діабет після трансплантації - сучасний рівень. Ланцет Діабет Ендокринол. 2016; 4 (4): 337-349.
Sharif A, Hecking M, de Vries AP та ін. Матеріали міжнародної консенсусної зустрічіпосттрансплантаційнийЦукровий діабет: рекомендації та подальші напрямки. Am J Transplant. 2014;14(9):1992-2000.
Porrini EL, Díaz JM, Moreso F та ін. Клінічна еволюціяпосттрансплантаційнийцукровий діабет. Трансплантація нефролу. 2016;31(3):495-505.
Valderhaug TG, Hjelmesæth J, Hartmann A та ін. Зв'язок ранніх рівнів глюкози після трансплантації з віддаленою смертністю. Діабетологія. 2011;54(6):1341-1349.
Cosio FG, Kudva Y, van der Velde M та ін. Нова гіперглікемія та діабет пов’язані з підвищеним серцево-судинним ризиком післятрансплантація нирки. Kidney Int. 2005;67(6):2415-2421.
Eide IA, Halden TA, Hartmann A та ін. Ризик смертності при цукровому діабеті після трансплантації на основі діагностичних критеріїв рівня глюкози та HbA1c. Transpl Int. 2016; 29 (5): 568-578.
Seoane-Pillado MT, Pita-Fernandez S, Valdes-Canedo F, et al. ~ Частота серцево-судинних подій і пов'язані з ними фактори ризику впересадка ниркипацієнти: аналіз виживання конкуруючих ризиків. BMC серцево-судинний розлад. 2017; 17 (1): 72.
Porrini E, Díaz JM, Moreso F та ін. Переддіабет є фактором ризику серцево-судинних захворювань після трансплантації нирки. Kidney Int. 2019;96(6):1374-1380.
Косіо Ф.Г., Песавенто Т.Є., Кім С., Осей К., Генрі М., Фергюсон Р.М. Виживаність пацієнтів після трансплантації нирки: IV. Вплив посттрансплантаційного діабету. Kidney Int. 2002;62(4): 1440-1446.
Dienemann T, Fujii N, Li Y та ін. Довгострокова виживаність пацієнтів і виживаність алотрансплантата нирки при цукровому діабеті після трансплантації: одноцентрове ретроспективне дослідження. Transpl Int. 2016; 29 (9): 1017-1028.
Kasiske BL, Snyder JJ, Gilbertson D, Matas AJ. Цукровий діабет післятрансплантація ниркиу Сполучених Штатах. Am J Transplant. 2003;3(2):178-185.
Ваутерс Р.П., Косіо Ф.Г., Суарес Фернандес М.Л., Кудва Ю., Шах П., Торрес В.Є. Серцево-судинні наслідки нової гіперглікемії післятрансплантація нирки. трансплантація. 2012;94(4):377-382.

