Розділ 1: Захист нирок за допомогою інгібіторів SGLT2: вплив на гостру та хронічну хворобу нирок
Jun 17, 2022
Для отримання додаткової інформації. контактtina.xiang@wecistanche.com
Анотація
Мета перегляду: Цей огляд пропонує критичну описову оцінку нових доказів того, що інгібітори котранспортера-2(SGLT2) натрію й глюкози мають нефропротекторну дію на людей із діабетом 2 типу.
Останні результати. Клас цукрознижуючих агентів, інгібіторів SGLT2, нещодавно продемонстрував сприятливий вплив на зменшення виникнення та прогресування ниркових ускладнень у людей з діабетом та без нього. Рандомізовані клінічні випробування та обсерваційні дослідження в «реальному світі», переважно за участю пацієнтів з цукровим діабетом 2 типу, відзначили, що використання інгібіторів SGLT2 може уповільнити зниження швидкості клубочкової фільтрації (ШКФ), зменшити виникнення мікроальбумінурії та уповільнити або повернути назад прогресування протеїнурії.
Резюме: Нефропротекторні ефекти інгібіторів SGLT2 є класовими ефектами, які спостерігаються для кожного із схвалених препаратів у людей з нормальною або порушеною ШКФ. Ці ефекти також спостерігаються у недіабетичних, худих і нормотензивних осіб, що свідчить про те, що механізми виходять за межі ефектів зниження рівня глюкози, зниження маси тіла та артеріального тиску, які супроводжують їх глюкозуричну дію у хворих на діабет. Ключовим механізмом є тубулогломерулярний зворотний зв’язок, у якому інгібітори SGLT2 змушують більше натрію проходити вздовж нефрону: натрій сприймається клітинами макули, які діють через аденозин, звужуючи аферентні клубочкові артеріоли, таким чином захищаючи клубочки шляхом зниження внутрішньоклубочкового тиску. Інші ефекти інгібіторів SGLT2 покращують канальцеву оксигенацію та метаболізм і зменшуютьзапалення нирокі фіброз. Інгібітори SGLT2 не підвищують ризик інфекцій сечовивідних шляхів або ризикгостре ураження нирок. Проте введення інгібітору SGLT2 пацієнтам із дуже низькою ШКФ не рекомендується через початкове зниження ШКФ, і доцільно припинити терапію у разі гострого порушення функції нирок, гіповолемії або гіпотензії.
Ключові слова: Інгібітори котранспортера-2(SGLT2) натрію та глюкози. Діабетична хвороба нирок. Хронічна хвороба нирок. Альбумінурія. Гостра хвороба нирок

Натисніть тут, щоб дізнатися, для чого використовується цистанх
вступ
Інгібітори натрій-глюкозного котранспортера-2(SGLT2) є цукрознижувальними агентами, які усувають надлишок глюкози через глюкозуричний ефект шляхом зменшення реабсорбції глюкози з ниркового фільтрату [1, 2e]. З моменту появи першого інгібітора SGLT2 у 2012 році цей клас розширився до канагліфлозину, дапагліфлозину, емпагліфлозину та ертугліфлозину в Європі та Америці, а в інших регіонах з’явилися додаткові представники класу (табл. 1). Незважаючи на те, що інгібітори SGLT2 призначені для зниження гіперглікемії та сприяння контролю маси тіла при діабеті 2 типу, зараз визнаються додаткові терапевтичні можливості для лікування серцево-ниркових ускладнень і супутніх захворювань діабету 2 типу.

Початкові побоювання щодо інгібіторів SGLT2 були зосереджені на можливому шкідливому впливі на ниркову систему, зокрема на посиленні сечостатевих інфекцій, погіршенні здоров’я сечового міхура та посиленні гострого ураження нирок [3]. Було також з побоюванням відзначено, що введення інгібітора SGLT2 спричинило тимчасове зниження швидкості клубочкової фільтрації та спричинило стійке зниження об’єму плазми та артеріального тиску. Проте спостереження під чассерцево-судинноїВипробування результатів і дослідження в реальному світі виявили потенційно сприятливі ефекти інгібіторів SGLT2 для зниження ризику виникнення та прогресування деяких серцево-судинних захворювань і збереженняфункції нирок.
Цей наративний огляд, який базується на обширному огляді літератури (вставка 1), пропонує критичну оцінку нових доказів нефропротекторних властивостей інгібіторів SGLT2. Блок 1 Стратегія пошуку літератури та критерії відбору. У MEDLINE, PubMed і Google Scholar проводився пошук статей, опублікованих у період з січня 2010 року по березень 2021 року, з використанням термінів «інгібітор транспортера натрію-глюкози», «інгібітор SGLT2 та загальні назви окремих інгібіторів SGLT2 у поєднанні з терміном «захворювання нирок», гостре ураження нирок, «хронічна хвороба нирок», 'функції нирок', 'діабет і 'діабет 2 типу. Дослідження були відібрані, якщо вони проводилися на людях і/або описували клінічно значущі механізми, були опубліковані англійською мовою та надавали переконливу інформацію. Звіти про випадки, редакційні статті, настанови та доклінічні дослідження були включені, коли вони пропонували інформацію або тлумачення, недоступні в інших джерелах.

Інгібування SGLT2
Розвиток інгібіторів SGLT2 можна простежити за спостереженнями дев'ятнадцятого сторіччя про те, що глюкозид флоризин викликав глюкозурію [4]. Доклінічні дослідження у 1980-х роках показали, що лікування флоризином могло контролювати гіперглікемію у щурів із частковою резекцією підшлункової залози, але клінічне застосування чекало синтетичних аналогів, які уникали розпаду кишкової глюкозидази та пропонували покращену ефективність та селективність інгібування SGLT2, а не SGLT1 [5,6].
SGLT2 міститься майже виключно в люмінальних мембранах епітеліальних клітин, що вистилають перший і другий сегменти проксимальних канальців, де він опосередковує реабсорбцію більшості (як правило, більше або дорівнює 90 відсоткам) відфільтрованої глюкози (рис. 1). SGLT1 в люмінальних мембранах клітин, що вистилають третій (прямий) сегмент проксимальних канальців, опосередковує реабсорбцію низьких концентрацій глюкози, що залишається в канальцях. SGLT1 найбільш поширений в апікальних мембранах ентероцитів, де він опосередковує поглинання глюкози з просвіту кишечника. Щоб уникнути перешкоджання всмоктуванню глюкози в кишечнику, перевага віддається високій селективності інгібування SGLT2 (табл. 1). Однак канагліфлозин певною мірою пригнічує SGLT1, а сотагліфлозин є інгібітором SGLT1/2: обидва ці агенти можуть уповільнювати всмоктування глюкози в кишечнику перед її всмоктуванням або деградацією, що сприяє прандіальному контролю глікемії. Кількості цих агентів, які абсорбуються та піддаються впливу нирок, інгібуючи SGLT2, недостатні, щоб мати будь-який істотний інгібуючий ефект на SGLT1 у проксимальних канальцях.

Рис.1 Ключові місця дії інгібіторів натрій-глюкозного котранспортера (SGLT). SGLT2 (кодується геном-носієм розчиненої речовини slcSa2) майже повністю експресується в люмінальній мембрані епітеліальних клітин, що вистилають перший і другий сегменти проксимальних канальців. Це високоємний котранспортер, що діє зі стехіометрією натрій-глюкоза 1:1, опосередковуючи реабсорбцію більшої частини відфільтрованої глюкози. SGLT1 (кодується slcSal) експресується в люмінальній мембрані клітин, що вистилають третій (прямий) сегмент проксимальних канальців. Він діє зі стехіометрією натрій-глюкоза 2:1 і має нижчу здатність, але вищу спорідненість, ніж SGLT2, для отримання низьких концентрацій глюкози, що залишається в канальці. SGLT1 широко експресується і зустрічається найбільше в апікальних мембранах ентероцитів у тонкій кишці, де він опосередковує поглинання глюкози з просвіту кишки. Обидва транспортери є вторинними активними симпортерами, які залежать від градієнта натрію, створеного Na плюс -K十-АТФазними насосами в базолатеральних мембранах, які знижують внутрішньоклітинну концентрацію натрію. Глюкоза, яка поглинається натрій-глюкозними котранспортерами в клітини проксимальних канальців і ентероцити, виводиться через базолатеральні мембрани та в інтерстицій за допомогою сприятливих транспортерів глюкози (наприклад, GLUT1 і GLUT2).
Гіперглікемія при цукровому діабеті означає, що кількість глюкози, яка перевищує норму, фільтрується з клубочків у проксимальні канальці, а збільшена кількість глюкози реабсорбується, що пов’язано з компенсаторною регуляцією експресії SGLT2 та SGLT1 [9]. Тим не менш, нирковий поріг для глюкози часто порушується, і глюкозурія посилюється інгібіторами SGLT2, які діють шляхом оборотного конкурентного інгібування без транспортування [2e]. Вони зв’язуються з котранспортерами на поверхні просвіту з більшою спорідненістю, ніж глюкоза, і з часом перебування в них кілька хвилин. Таким чином, тривіальна (терапевтична) концентрація інгібітора SGLT у фільтраті може запобігти реабсорбції великої (приблизно до 100 г/день) кількості відфільтрованої глюкози. Хоча інгібітори SGLT2 знижують нирковий поріг для глюкози, їх глюкозуричний ефект є самообмежуваним, тому вони не піддають ризику клінічно значущої гіпоглікемії. Це пояснюється тим, що, оскільки інгібітор збільшує глюкозурію, це знижує рівень глюкози в крові, так що фільтрується менше глюкози, і достатня кількість активних (незагальмованих) транспортерів може потім реабсорбувати (майже всю цю меншу кількість глюкози, що запобігає зниженню рівня глюкози в крові нижче рівня евглікемії).
Зниження рівня глюкози та зниження ваги. Активність інгібіторів SGLT2 не залежить від статусу інсуліну, тобто не послаблюється резистентністю до інсуліну або абсолютною нестачею інсуліну, що дозволяє знижувати рівень глюкози при діабеті 2 та 1 типу. Залежність від ступеня гіперглікемії означає, що цукрознижувальна ефективність більша в осіб із вищими концентраціями глюкози в крові та особливо корисна для зменшення коливань глюкози після їжі. Мета-аналіз зниження рівня HbAlc за допомогою інгібіторів SGLT2 при цукровому діабеті 2 типу постійно відзначав зниження приблизно на 0.5–1 відсоток (6-11 ммоль/моль) порівняно з вихідним рівнем приблизно на 8 відсотків (64 ммоль/моль). моль)[10-12]. Оскільки інгібітори SGLT2 мають інший механізм дії, ніж інші цукрознижувальні агенти, їх можна використовувати в комбінації з іншими агентами, включаючи інсулін, і часто можуть зменшити кількість інсуліну, необхідного при цукровому діабеті 2 та 1 типу [13,14]. Однак інгібітори SGLT2 не можуть замінити потребу в достатній кількості інсуліну для підтримки основних метаболічних потреб. Надмірне зниження (або затримка введення) інсуліну зазвичай є причиною атипового (еуглікемічного) діабетичного кетоацидозу (ДКА), при якому ДКА виникає без гіперглікемії та іноді виявляє, що діагноз діабету 2 типу є 1 типом [15].
In clinical trials with type 2 diabetes patients, the weight-reducing effect of SGLT2 inhibitors has typically been around 3 kg, leveling out by 6-12 months, although 'real-world observational studies have often noted reduc-tions>6 кг, що триває більше року. Зниження ваги, як правило, пояснюється втратою калорій через глюкозурію. Таблиця 2. Великі рандомізовані контрольовані серцево-судинні дослідження (CVOTs), у яких ниркові події вимірювалися під час лікування пацієнтів з діабетом 2 типу інгібітором SGLT2. ІМТ, оцінка серцево-судинних захворювань, ССЗ швидкість клубочкової фільтрації, цукрознижуючий препарат GLD, основна несприятлива серцево-судинна подія MACE (серцево-судинна смерть, нефатальний інфаркт міокарда або інсульт), інфаркт міокарда ІМ, UACR співвідношення альбумін-креатинін у сечі. Значення MACE, серцево-судинної смерті, інфаркту міокарда, інсульту, серцевої недостатності, усіх смертельних випадків і ниркової складової є коефіцієнтами ризику з 95-відсотковим довірчим інтервалом.* Ниркові композити відрізнялися між дослідженнями: EMPA-REG зменшує жирову масу, хоча зменшений об’єм плазми також може сприяти [16, 17].

Table2 Large randomized controlled cardiovascular outcome trials(CVOTs)in which renal events were measured during treatment of type 2 diabetes patients with an SGLT2 inhibitor.BM7 body mass index, CVD cardiovascular disease,eGFR estimated glomerular filtration rate, GLD glucose-lowering drug, MACE major adverse cardiovascular event(cardiovascular death, non-fatal myocardial infarction or stroke), MI/ myocardial infarction, UACR urine albumin-creatinine ratio. Values for MACE, CV death, MI, stroke, heart failure, all deaths, and renal composite are hazard ratios with 95% confidence intervals.*Renal composites varied between trials: EMPA-REG OUTCOMES.doubling of serum creatinine,eGFR≤45 ml/min/1.73 m², start renal replacement, renal death; CANVAS PROGRAM,>40% decrease in eGFR, start renal replacement, renal death: DECLARE,>40% decrease in eGFR,end-stage kidney disease, renal or CV death; VERTIS, doubling of serum creatinine, start renal replacement, renal death; CREDENCE, double serum creatinine,end-stage kidney disease, renal death or CV death: SCORED, sustained (>30 days)decrease of≥50%in eGFR, dialysis, and renal transplantation or sustained (>30 днів) рШКФ<15 ml/min/1.73="" m².**decline="" in="" the="" long-term="" rate="" of="">

Серцево-судинні ефекти
Beyond glucose-lowering and weight lowering, SGLT2 inhibitors have consistently reduced blood pressure (systolic by 3-5 mmHg and diastolic by 2-3 mmHg)during clinical trials without causing hypotension [18]. SGLT2 inhibitors have also OUTCOMES, doubling of serum creatinine, eGFR≤45 ml/min/1.73 m², start renal replacement, renal death; CANVAS PROGRAM,>40% decrease in eGFR, start renal replacement, renal death: DECLARE,>40% decrease in eGFR, end-stage kidney disease, renal or CV death; VERTIS, doubling of serum creatinine, start renal replacement, renal death; CREDENCE, double serum creatinine,end-stage kidney disease, renal death or CV death; SCORED, sustained(>30 days)decrease of≥50% in eGFR, dialysis, and renal transplantation or sustained(>30 днів) рШКФ<15 ml/min/1.73="" m².**declinein="" long-term="" rate="" of="" egfr="" consistently="" reduced="" the="" risk="" of="" new="" heart="" failure="" and="" worsening="" of="" existing="" heart="" failure="" during="" clinical="" trials="" (table2).="" the="" benefit="" is="" evident="" within="" a="" few="" weeks="" of="" starting="" an="" sglt2="" inhibitor,="" occurs="" in="" people="" with="" and="" without="" diabetes,="" and="" is="" independent="" of="" the="" extent="" of="" effects="" on="" glucose,="" weight,="" or="" blood="" pressure[19-21].="" the="" improved="" prognosis="" for="" heart="" failure="" is="" also="" independent="" of="" age="" and="" is="" not="" significantly="" affected="" by="" the="" presence="" of="" ckd,="" albuminuria,="" or="" concomitant="" use="" of="" antihypertensive="" therapies.="" studies="" in="" which="" ejection="" fraction="" was="" quantified="" have="" mostly="" involved="" patients="" with="" reduced="" ejection="" fraction(hfref),="" but="" there="" is="" emerging="" evidence="" that="" sglt2="" inhibitors="" can="" also="" benefit="" those="" with="" preserved="" and="" mid-range="" ejection="" fraction.[22-25].measures="" of="" atherosclerotic="" cardiovascular="" disease(cardiovascular="" deaths,="" non-fatal="" myocardial="" infarction,="" and="" stroke)="" have="" also="" been="" reduced="" in="" some="" studies="" with="" sglt2="" inhibitors:="" these="" are="" reviewed="" in="" detail="" elsewhere="" in="" the="" context="" of="" the="" reciprocating="" interrelationships="" of="" heart="" and="" kidney="">
Діабетична хвороба нирок
Усі типи діабету пов’язані з підвищеним ризиком порушення функції нирок (так званої діабетичної нефропатії або діабетичної хвороби нирок (ДЗН)). Це зазвичай розпізнається за прогресуючою хронічною хворобою нирок (ХНН) з приблизною швидкістю клубочкової фільтрації (eGFR)<60 ml/min/1.73m²that="" can="" be="" attributed="" to="" diabetes="" [28].="" the="" condition="" may="" be="" accompanied="" by="" micro-(uacr="" 30-300="" mg/g)or="" macro-(="">300 mg/g) albuminuria, often with an underlying glomerulopathy of thickened capillary basement membranes, diffuse mesangial sclerosis, and nodular sclerosis. The normal age-related rate of decline in eGFR(~1 ml/min/l.73m²per year wheneGFR>60 мл/хв/1,73 м²) зазвичай подвоюється при цукровому діабеті 2 типу з ХХН і може перевищувати 3 мл/хв/1,73 м² на рік у осіб з макроальбумінурією [29]. Обсерваційні дослідження показують, що 20-40 відсотків людей із діабетом 2 типу мають рШКФ<60 ml/min/1.73m²,="" mostly="" amongst="" older="" patients="" and="" those="" with="" poor="" glycaemic="" control.="" type="" 2="" diabetes="" is="" also="" a="" major="" cause="" of="" end-stage="" kidney="" disease(eskd)="" requiring="" renal="" replacement="" therapy="">
Звичайні методи лікування (здебільшого суворий контроль артеріального тиску за допомогою інгібіторів АПФ або БРА та інтенсивний контроль рівня глюкози в крові) зменшують прогресування DKD, але вони не можуть зупинити прогресування захворювання. Зараз з’являється величезна кількість доказів, які свідчать про те, що інгібітори SGLT2 можуть захищати від виникнення DKD і уповільнювати прогресування захворювання незалежно від блокади ренін-ангіотензин-альдостеронової системи (РААС) і разом з нею.

Захворювання нирок і використання інгібіторів SGLT2
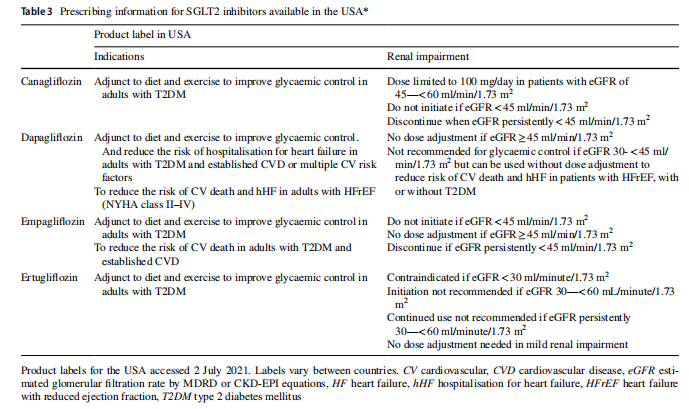
Оскільки зниження ШКФ зменшує кількість глюкози, що доставляється в проксимальні канальці, глюкозурична ефективність (і, отже, антигіперглікемічна ефективність) інгібіторів SGLT2 знижується приблизно відповідно до зниження ШКФ. Як наслідок, на етикетках продуктів для інгібіторів SGLT2 вказані значення ШКФ. нижче якого рекомендовано не розпочинати або продовжувати лікування [35-38]. Зі зростанням усвідомлення того, що інгібітори SGLT2 не загрожують нирковій безпеці та забезпечують кардіо-ниркову користь, показання та дозволені діапазони eGFR були розширені (табл. 3) і відрізняються між країнами.
Ниркові кінцеві точки
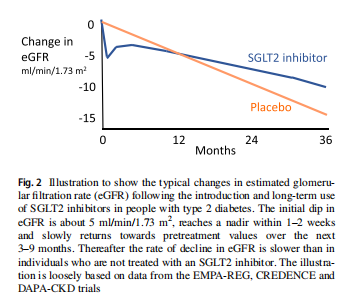
Визнання того, що інгібітори SGLT2 можуть змінити перебіг діабетичної хвороби нирок, спочатку було затьмарено короткочасними спостереженнями, зосередженими на початковому падінні eGFR. Це падіння зазвичай становить близько 5 мл/хв/1,73 м², досягаючи найнижчої позначки протягом 1-2 тижнів і повільно повертаючись до значень перед обробкою протягом наступних 3-9 місяців (рис. 2). Проте дані довготривалих досліджень діабету 2 типу, зокрема постмаркетингових досліджень серцево-судинних результатів (CVOT), описаних нижче, показали, що eGFR згодом знижувалася повільніше при застосуванні інгібітору SGLT2, ніж при лікуванні плацебо пацієнтів і що альбумінурія була менш тяжкою.
Заздалегідь визначені вторинні кінцеві точки в CVOT оцінювали різні індивідуальні та комплексні показники функції нирок, які включали прогресування альбумінурії (вказується UACR), подвоєння рівня креатиніну сироватки, зниження eGFR (до будь-якого<45><60 ml/min/1.73m²),="" end-stage="" kidney="" disease,="" kidney-related="" death="" or="" renal="" replacement="" therapy="" (dialysis="" or="" transplantation).="" because="" the="" composites="" and="" the="" patient="" populations="" differed="" between="" the="" trials,="" direct="" comparisons="" are="" necessarily="" cautious.="" however,="" each="" of="" the="" composites="" that="" included="" a="" measure="" of="" the="" rate="" of="" decline="" in="" egfr="" noted="" a="" significant="" benefit="" of="" treatment="" with="" an="" sglt2="" inhibitor:="" for="" example,="" a="" decrease="" in="" adverse="" events="" by≥30%(table="" 2).="" also,="" the="" individual="" renal="" parameters="" assessed="" in="" the="" cvots="" showed="" either="" significant="" reductions="" or="" non-significant="" numerical="" reductions="" in="" the="" occurrence="" of="" adverse="" renal="" events,="" bearing="" in="" mind="" that="" the="" studies="" were="" not="" powered="" for="" renal="">
Large Randomised Trials in Type 2 Diabetes In the EMPA-REG OUTCOME trial, the renal composite (doubling of serum creatinine,eGFR≤45 ml/min/1.73 m², initiation of renal replacement therapy or death from kidney disease) was reduced by 46% in the groups receiving empagliflozin [39,40]. After the initial dip in eGFR, there was a slight annual decline in eGFR with the use of empagliflozin (0.19±0.11 ml/min/1.73 m²/year; mean±standard error)compared with a more rapid decline in the placebo group (1.67±0.13 mL/min/1.73 m²/year). Progression to macroalbuminuria (UACR>300 мг/г) було знижено на 38 відсотків із застосуванням емпагліфлозину, а також спостерігалося значне зменшення кількості пацієнтів із подвоєнням рівня креатиніну в сироватці крові, зниженням eGFR до 45 мл/хв/1,73 м² або менше, ніж і початок замісної ниркової терапії.
Дослідження DECLARE-TIMI 58 виявило, що застосування дапагліфлозину було пов’язане зі зниженням ниркової композиції на 47 відсотків, тобто стійким зниженням eGFR на 40 відсотків або більше.<60 ml/min/1.73="" m²,="" new="" eskd="" or="" death="" from="" a="" renal="" cause.="" the="" decline="" in=""><60 ml/min/1.73="" m²)="" was="" 46%="" less="" with="" dapagliflozin,="" and="" there="" were="" also="" significant="" reductions="" in="" eskd="" and="" renal="" death.="" additionally,="" dapagliflozin="" decreased="" new-onset="" albuminuria="" by="" 21%="" and="" new-onset="" macroalbuminuria="" by="">
Комбінований аналіз випробувань CANVAS і CANVAS-R (програма CANVAS) відзначив, що використання канагліфлозину знижує на 40 відсотків ниркову комплексну стійку (22 послідовні вимірювання) зниження (більше або дорівнює 40 відсоткам) потреби в eGFR замісна ниркова терапія або смерть від ниркових причин [43]. Прогресування альбумінурії (зміни від нормальної до мікро- або мікро- до макро-альбумінурії або більше ніж або дорівнює 30-відсотковому збільшенню мікро-альбумінурії) було зменшено за допомогою канагліфлозину на 27 відсотків, і багато пацієнтів, які отримували канагліфлозин, показали зниження мікро- або макроальбумінурія.
У дослідженні VERTIS CV нирковий композит, який не включав вимірювання eGFR (подвоєння креатиніну сироватки, початок замісної ниркової терапії або смерть від ниркової причини), був чисельно зменшений на 19 відсотків (статистично незначно) на застосування ертугліфлозину [44]. Однак окремий аналіз ниркового композиту, що включає стійке зниження eGFR більше або дорівнює 40%, нирковий діаліз/трансплантація або ниркова смерть, відзначив 34-відсоткове зниження при застосуванні ертугліфлозину, а через 5 років — зниження eGFR був значно меншим (на 2,6 мл/хв/1,73 м²), ніж у плацебо. Крім того, за 5 років ертугліфлозин зменшив прогресування від нормальної до мікроальбумінурії на 21 відсоток і збільшив регресію від макро- до мікро- та від макро- або мікро- до нормоальбумінурії на 23 відсотки.
Декілька метааналізів ниркових даних із вищезазначених CVOT та інших досліджень підтвердили, що інгібітори SGLT2 зменшили сукупний показник погіршення eGFR, ESKD або ниркової смерті приблизно на 33 відсотки [46-48].
Дослідження за участю людей із порушенням ниркового статусу У чотирьох CVOT, описаних вище, сприятливий вплив інгібітора SGLT2 на різні параметри нирок був очевидним (більшою чи меншою мірою) незалежно від статі, етнічного походження, віку, ваги, тривалості чи тяжкості захворювання. діабет; наявність або відсутність серцево-судинних захворювань; і базову рШКФ або вихідну альбумінурію. Однак у цих дослідженнях небагато пацієнтів мали прогресуючу ХХН (egeGFR<45 ml/min/1.73="" m²)or="" advanced="" macroalbuminuria.="" this="" was="" addressed="" in="" the="" credence="" study="" in="" which="" type="" 2="" diabetes="" patients="" were="" recruited="" with="" an="" egfr="" range="" of="" 30-90="" ml/min/1.73="" m²,="" macroalbuminuria(uacr="">300 до<5,000 mg/g),="" and="" raas="" blockade="">
У CREDENCE 60 відсотків пацієнтів мали eGFR<60 ml/min/1.73="" m²,and="" 30%="" had="" anegfr=""><45ml in/1.73="" m²(mean="" baseline="" egfr="" of="" 56="" ml/min/1.73="" m2),while="" 88%="" had="" a="" uacr="">{{0}} мг/г (медіана UACR 927 мг/г). Композитний нирковий показник (подвоєння сироваткового креатиніну, ESKD, ниркова смерть або серцево-судинна смерть) був на 30 відсотки нижчим із використання канагліфлозину, і спостерігалося значне зниження швидкості зниження eGFR для тих, хто отримував канагліфлозин, порівняно з плацебо (-1.85±0.13 проти -4.59±0.14 мл/хв/1,73 м² Якщо ці різні темпи зниження eGFR продовжуватимуться для такої популяції (вік 63 роки, eGFR 56 мл/хв/1,73 м²), за підрахунками знадобиться понад 10 років більше для пацієнтів, які приймають канагліфлозин, щоб прогресувати до ESKN. [49] Дійсно, у CREDENCE було на 32 відсотки менше випадків ESKD (eGFR<15 ml/min/1.73="" and/or="" renal="" replacement)="" and="" 34%="" fewer="" renal="" deaths="" with="" the="" use="" of="" canagliflozin.="" also,="" canagliflozin="" lowered="" uacr="" by="" 31%="" at="" 6="" months="" and="" increased="" by="" 30%="" the="" number="" of="" patients="" with="" a="" reduction="" in="" uacr[50].="" of="" particular="" note,="" the="" effectiveness="" of="" the="" sglt2="" inhibitor="" to="" slow="" the="" decline="" in="" egfr="" and="" reduce="" the="" progression="" of="" albuminuria="" was="" similar="" for="" patients="" with="" a="" baseline="" egfr="">або<45 ml/min/1.73="" m²and="" a="" uacr="">або<1,000 mg/g,="" and="" the="" sglt2="" inhibitor="" also="" slowed="" the="" decline="" in="" egfr="" for="" patients="" with="" a="" baseline=""><30 ml/min/1.73m².="" the="" effectiveness="" of="" the="" sglt2="" inhibitor="" on="" these="" parameters="" was="" independent="" of="" glycaemic="" status,="" type="" of="" raas="" blockade,="" and="" atherosclerotic="" cardiovascular="" disease,="" suggesting="" that="" the="" benefits="" of="" sglt2="" inhibitors="" on="" renal="" function="" can="" be="" gained="" irrespective="" of="" cardio-renal="" or="" metabolic="" status="" in="" type="" 2="">
Similar findings emerged from the SCORED trial in type 2 diabetes patients with CKD (eGFR 25-60 ml/min/1.73 m²). Treatment with the SGLT1/2 inhibitor sotagliflozin was associated with a 29% reduction in the renal composite of sustained (>30 days) decrease of≥50% in eGFR,dial-ysis, renal transplantation or sustained(>30 днів) рШКФ<15 ml/min/1.73="">
Because the CVOTs and similar studies in type 2 diabetes indicated that the cardio-renal benefits of SGLT2 inhibitors were not contingent on their glucose-lowering efficacy, studies were undertaken in populations that included people without diabetes(Table 4).The DAPA-CKD trial examined the effect of dapagliflozin in people with(67%)and with-out(33%)type 2 diabetes who had renal impairment (eGFR 25-75ml/min/1.73 m²,mean 43.1 ml/min/1.73 m²; and UACR 200-5000 mg/g,median~950 mg/g with 48.3% of patients having a UACR>1000 mg/g)[51].Standard care for all patients included RAAS blockade. Similar reductions in the renal composite endpoint(decline in eGFR>50%, ESKD, renal death, or CV death) were observed with the use of dapagliflozin in those with (by 36%)and without(by 50%)diabetes. Dapagliflozin also reduced each of the component measures of the composite, and the findings were generally consistent for patients with an eGFR>або<45 ml/min/1.73="" m²or="" uacr="">або<1,000 mg/g.="" the="" average="" annual="" decline="" in="" egfr="" was="" also="" slower="" with="" dapagliflozin="" than="" with="" placebo="" (-1.67="" versus-3.59="" ml/min/1.73="">
